Matura 2016: Chemia rozszerzona [ODPOWIEDZI, ARKUSZ CKE]
W piątek, 13 maja, maturzyści zdawali egzamin maturalny z chemii. O godzinie 9 rozpoczęła się matura 2016 z chemii na poziomie rozszerzonym.
Jak Wam poszło? Możecie to sprawdzić na naszej stronie!
Matura 2016 - harmonogram
Sprawdź też: Matura 2016: CHEMIA rozszerzona i wszystkie inne przedmioty [ODPOWIEDZI, ARKUSZ CKE]
Matura 2016: CHEMIA rozszerzona - ODPOWIEDZI:
ODPOWIEDZI ZACZNĄ SIĘ TU POJAWIAĆ PO GODZINIE 14, KIEDY CKE OPUBLIKUJE ARKUSZ EGZAMINACYJNY.
Zadanie 1.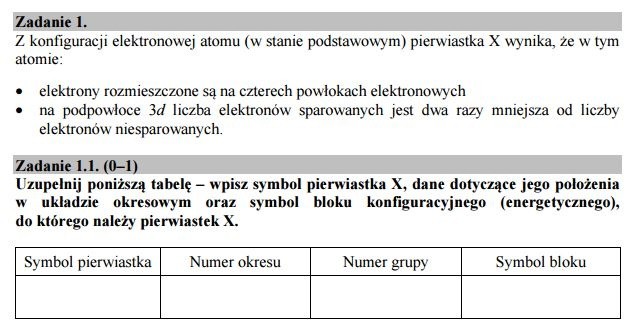
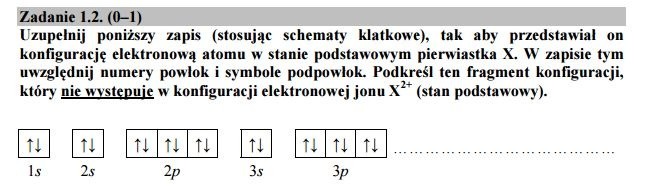
Odpowiedź:
Zadanie 1.1
Symbol: Fe
Numer okresu: 4
Nr grupy: 8
Symbol bloku: d
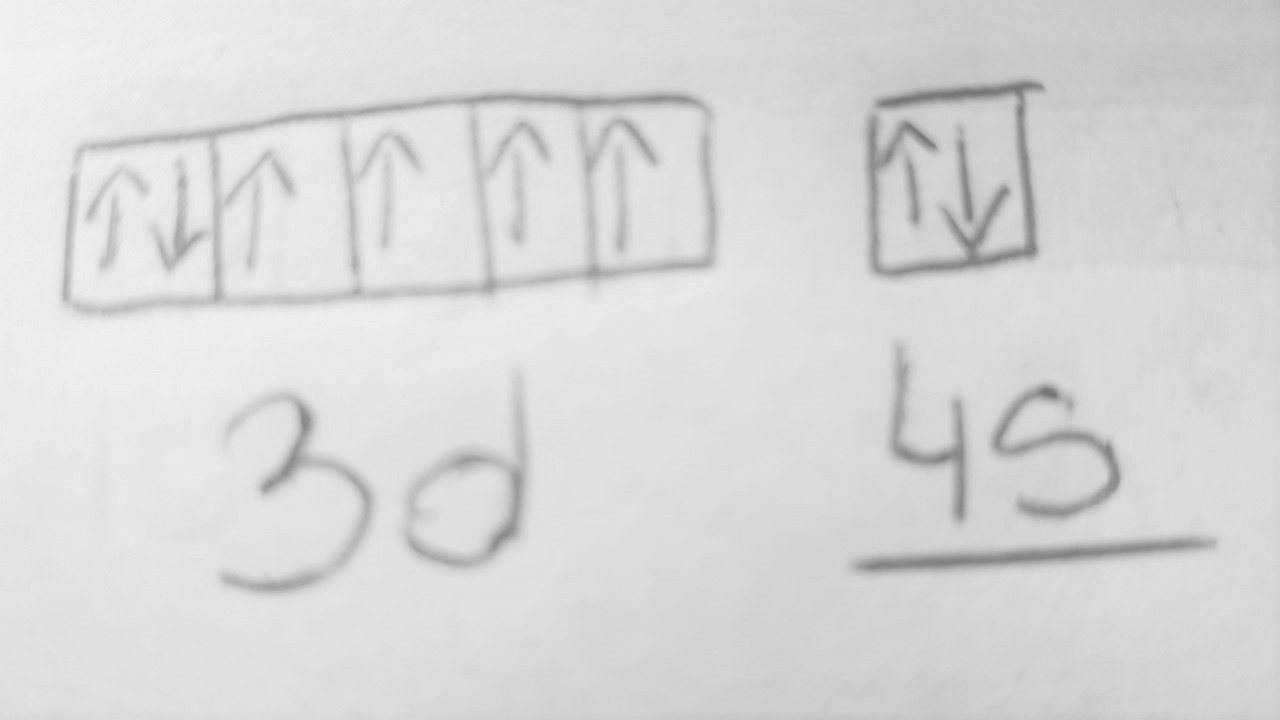
Zadanie 2.
Odpowiedź:
1.FAŁSZ
2.PRAWDA
3.PRAWDA
Zadanie 3-4.
Odpowiedź:
Zadanie 3.
1. dodatnio; dużą
2. wyższa; z silniejszego; większej
Odpowiedź:
Zadanie 4.
Zadanie 5.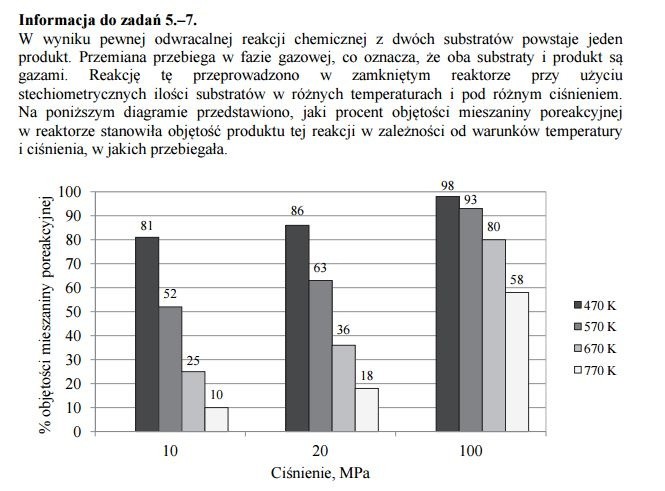

Odpowiedź:
Zadanie 5. Zadanie 6.
Zadanie 7-8
Odpowiedź:
Zadanie 7.
B
Zadanie 8.
1,34%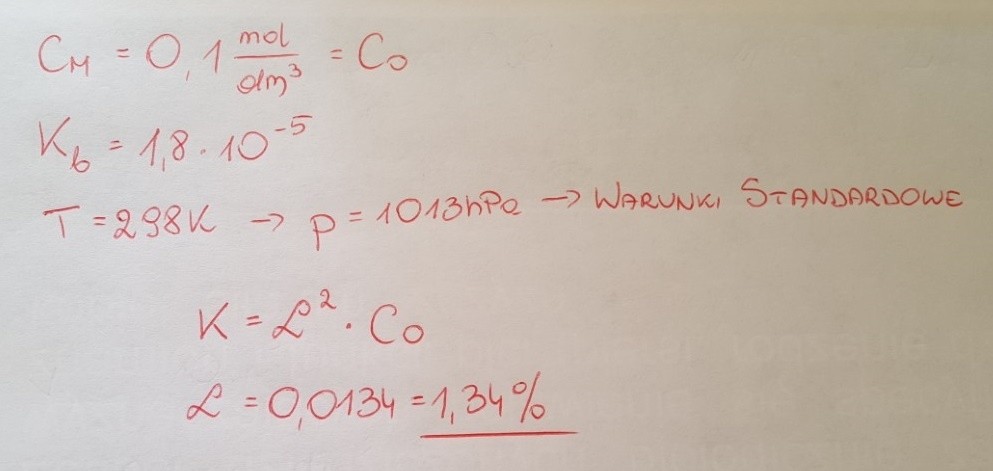
Zadanie 9.
Odpowiedź:
9.1 HCl
9.2 Przed: żółta; po: czerwona
Informacja do zadań 10.–11.
Jednym z tlenowych kwasów siarki jest kwas trioksotiosiarkowy (nazwa zwyczajowa: kwas tiosiarkowy) o wzorze H2S2O3. Anion 2− S2O3 (tiosiarczanowy) ma strukturę analogiczną do struktury jonu siarczanowego(VI), z tą różnicą, że zamiast jednego atomu tlenu zawiera atom siarki. Centralnemu atomowi siarki w jonie 2− S2O3 odpowiada stopień utlenienia (VI), a skrajnemu – stopień utlenienia (–II). Kwas tiosiarkowy jest substancją nietrwałą, trwałe są natomiast sole tego kwasu – tiosiarczany. Spośród tych soli największe znaczenie ma tiosiarczan sodu – zwykle występujący jako pentahydrat o wzorze Na2S2O3 · 5H2O. Znajduje on zastosowanie w przemyśle włókienniczym jako substancja służąca do usuwania resztek chloru używanego do bielenia tkanin. Podczas zachodzącej reakcji chlor utlenia jony 2− S2O3 do jonów siarczanowych(VI). W przemianie tej udział bierze również woda.
Na podstawie: A. Bielański, Podstawy chemii nieorganicznej, Warszawa 2004.

Odpowiedź:
10.1
Równanie reakcji redukcji: Cl2 (0st.utl) + 2e- -> 2Cl- (-Ist.utl)
Równanie reakcji utleniania: S2- (-IIst.utl) -> S (0st.utl) +2e-
10.2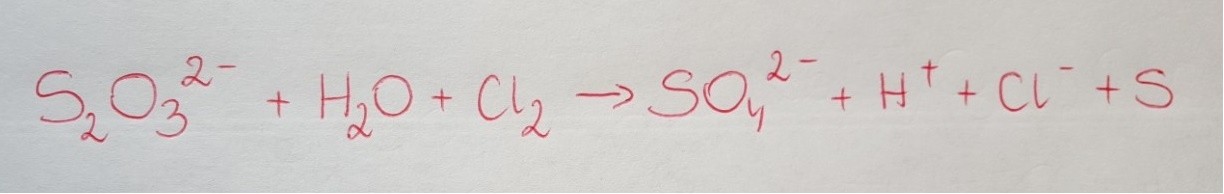
Zadanie 12.
Odpowiedź:
1. czerwień bromofenolowa
2. oranż metylowy, czerwień bromofenolowa, fenoloftaleina
Zadanie 13.
Odpowiedź:
obojętny, NaOH(kwasu), HCl(aq)
Zadanie 14-15.
Odpowiedź:
Zadanie 14.
Barwa wskaźnika po dodaniu 5 cm3 titranta: niebieski
Barwa wskaźnika po dodaniu 10 cm3 titranta: żółty
Barwa wskaźnika po dodaniu 15 cm3 titranta: czerwony
Zadanie 15.
C
Zadanie 16.
Zadanie 16.4.
Podaj nazwę metody, którą należy zastosować w celu wyodrębnienia wodnego roztworu kwasu siarkowego(VI) z mieszaniny poreakcyjnej.
Odpowiedź:
16.1
Zestaw odczynników I: H2S (g)
Zestaw odczynników II: CuSO4 (aq)
Zadanie 16.2.
Przed dodaniem odczynnika: klarowny niebieski roztwór
Po zajściu reakcji: odbarwienie roztworu, czarny osad
Zadanie 16.3.
Cu2+ + H2S -> CuS + 2H+
lub
Cu2+ + S2- => CuS
Zadanie 16.4.
filtracja lub dekantacja
Zadanie 17.
Odpowiedź:
Na+ + H2PO4- + H2O -> HPO42- + Na+ + H3O+
lub
NaH2PO4(s) + 2H2O => Na+ + 2H30+ + PO4-
Zadanie 18.
Odpowiedź:
H2PO4- + H3O+ -> H3PO4 + H2O
H2PO4- + OH- -> HPO42- + H2O
Zadanie 19.
Odpowiedź:
Nazwa wybranego odczynnika: KI (wodny roztwór jodku potasu)
Uzasadnienie: Osad AgI najsłabiej się rozpuszcza.
Po dodaniu do roztworu azotanu srebra roztworu jodku potasu wytrąci się jodek srebra - sól o najmniejszym z wymienionych iloczynie rozpuszczalności. Im mniejszy iloczyn rozpuszczalności tym substancja gorzej rozpuszczalna a więc mniej jonów zostanie dostarczonych do roztworu.
Zadanie 20.
Odpowiedź:
Odpowiedź: 13,1 g
Zadanie 21.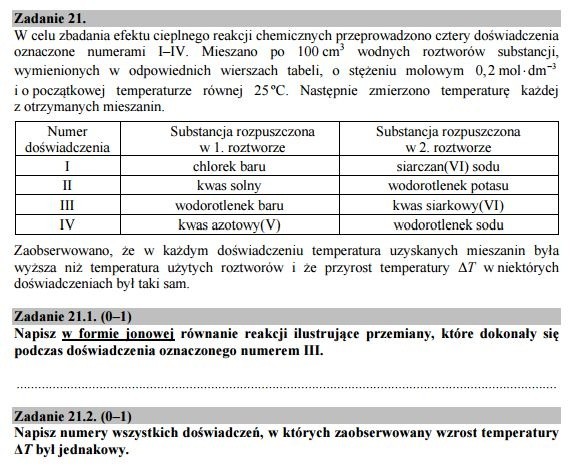
Odpowiedź:
21.1
Ba2+ + 2OH- + 2H+ + SO42- -> BaSO4 + 2H2O
21.2
II i IV
Zadanie 22.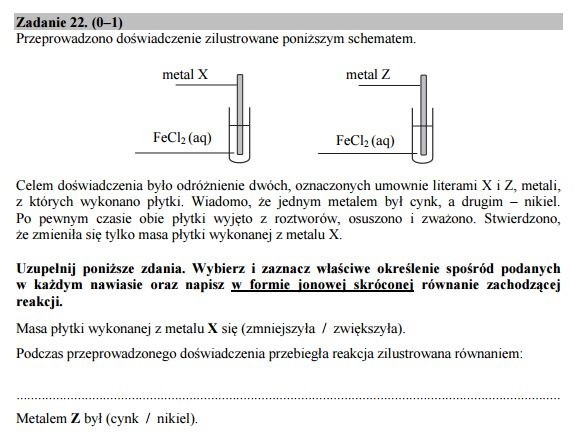
Odpowiedź:
zmniejszyła
Zn + Fe2+ -> Zn2+ + Fe
nikiel
Zadanie 23.
Odpowiedź:
C6H14
Zadanie 24.
Zadanie 24.2.
Podaj nazwy wszystkich związków organicznych, które powstały w wyniku utleniania alkenów A i B.
Odpowiedź:
24.1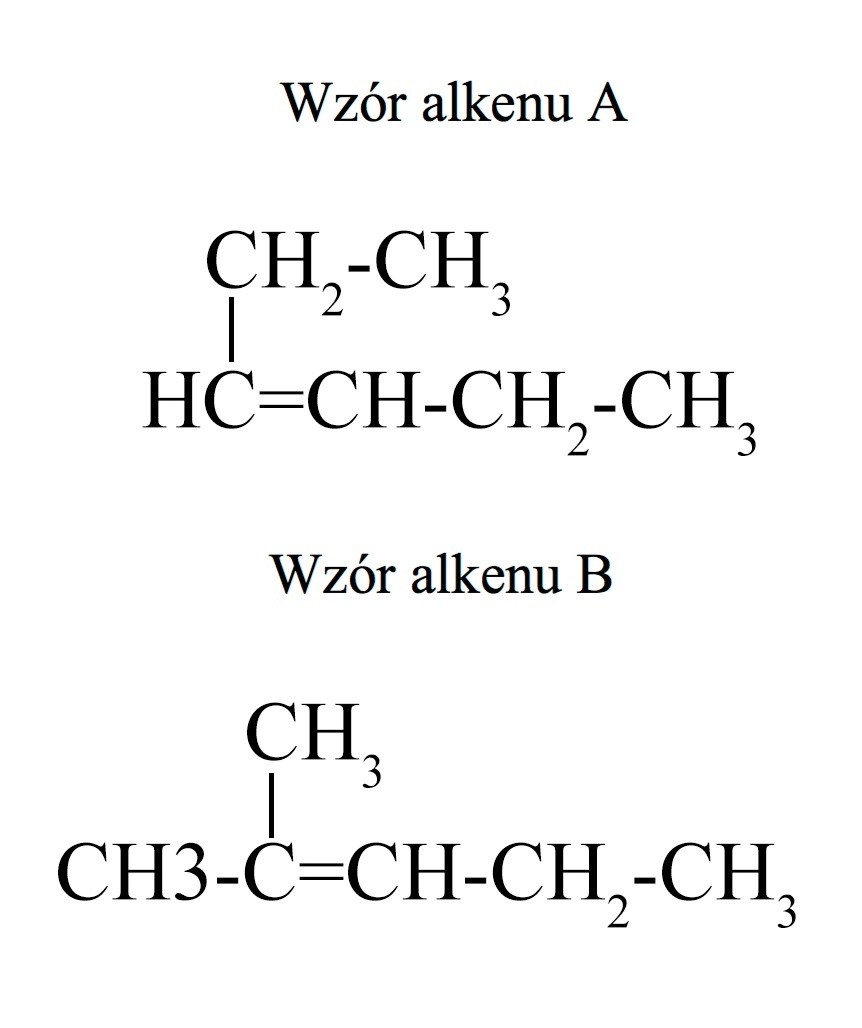
24.2
propanon, kwas propanowy
Zadanie 25.

Odpowiedź:
25.1
elektrofilowego
nukleofil
oddaje
25.2
Wybrane alkohole: CH3CH2CH2OH, CH3CH2CH2CH2OH
Uzasadnienie: Addycję wody do alkenów prowadzi się używając reguły Markownikowa, a ona wyklucza powstanie tych alkoholi.
Zadanie 26.
Odpowiedź:
Numer związku: I; brak asymetrycznego atomu węgla
Numer związku: II; forma mezo narysowanej cząsteczki
Zadanie 27 i 28.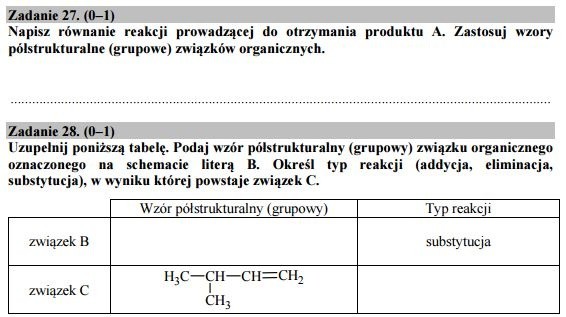
Odpowiedź:
Zadanie 27.
CH3CH(CH3)CH2CHO + H2 --kat--> CH3CH(CH3)CH2CH2OH
Zadanie 28.
związek B:
wzór: CH3-CH(CH3)-CH2-CH2Br
Typ reakcji: substytucja
związek C:
wzór: H3C-CH(CH3)CH=CH2;
Typ reakcji: eliminacja
Zadanie 29.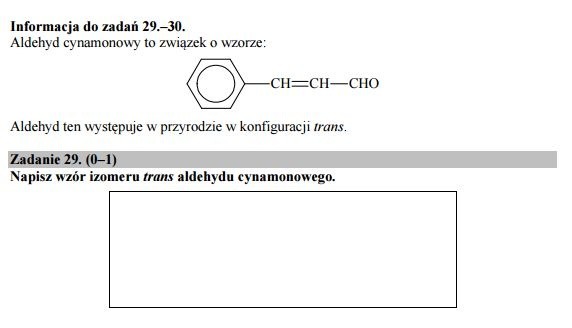
Odpowiedź: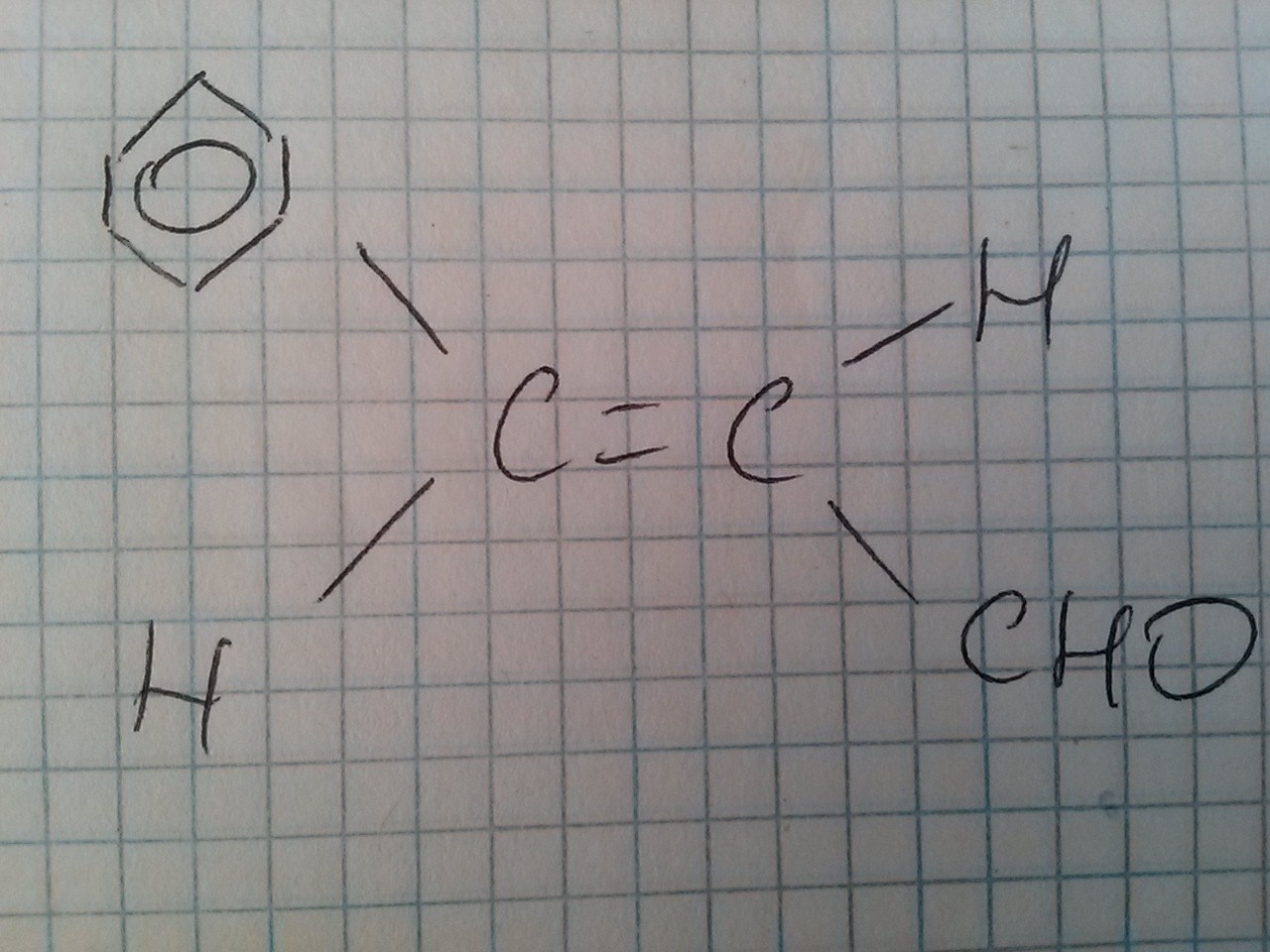
Zadanie 30.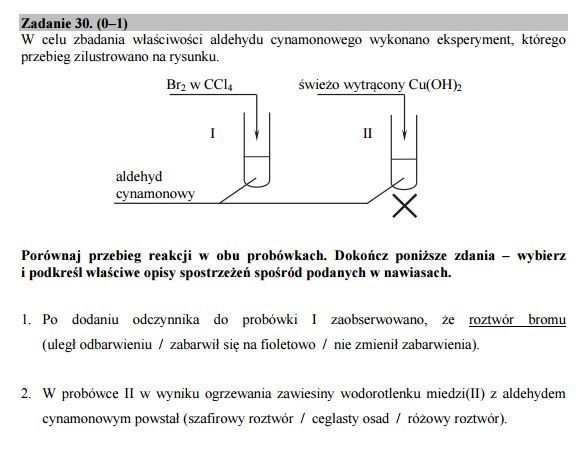
Odpowiedź:
uległ odbarwieniu
ceglasty osad
Zadanie 31.
Odpowiedź:
pH = 2,4
Wniosek: Wyższa wartości pH kwasów nie oznacza, że ma bardziej kwasowy odczyn, bo to zależy od stężenia roztworu kwasu
Zadanie 32.
Odpowiedź:
związek X: CH3COOH
Równanie: CH3CH(OH)COOH + CH3COOH = CH3-COO-C(CH3)-COOH + H2O
Zadanie 33 i 34.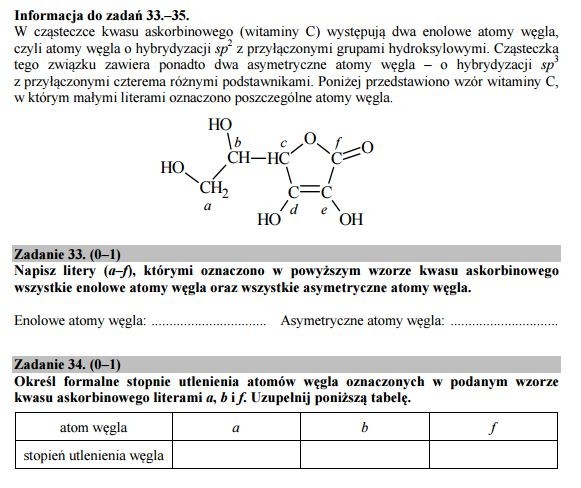
Odpowiedź:
Zadanie 33.
Enolowe atomy węgla: d, e
Asymetryczne atomy węgla: b, c
Zadanie 34.
Odpowiedź:
stopień utlenienia węgla : -I, 0, III
Zadanie 35.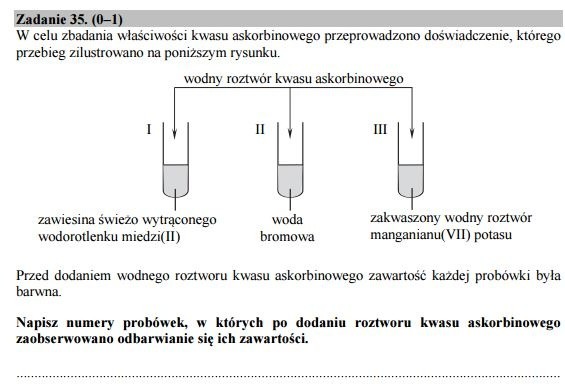
Odpowiedź:
II, III
Zadanie 36.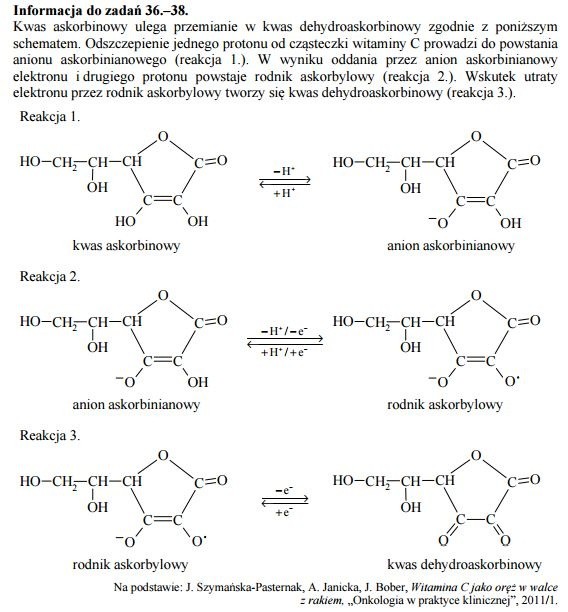
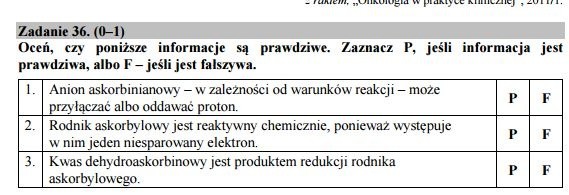
Odpowiedź:
1 PRAWDA
2 PRAWDA
3 FAŁSZ
Zadanie 37.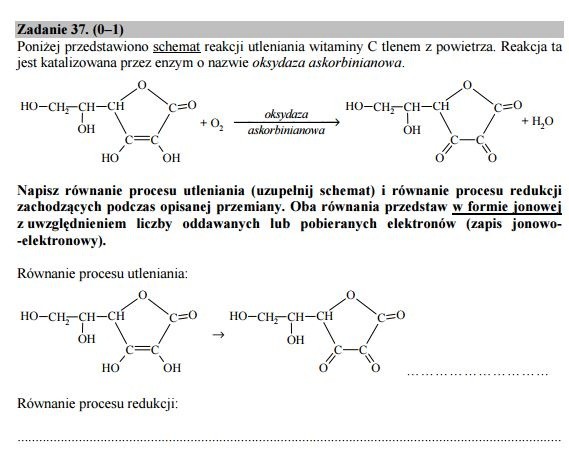
Odpowiedź: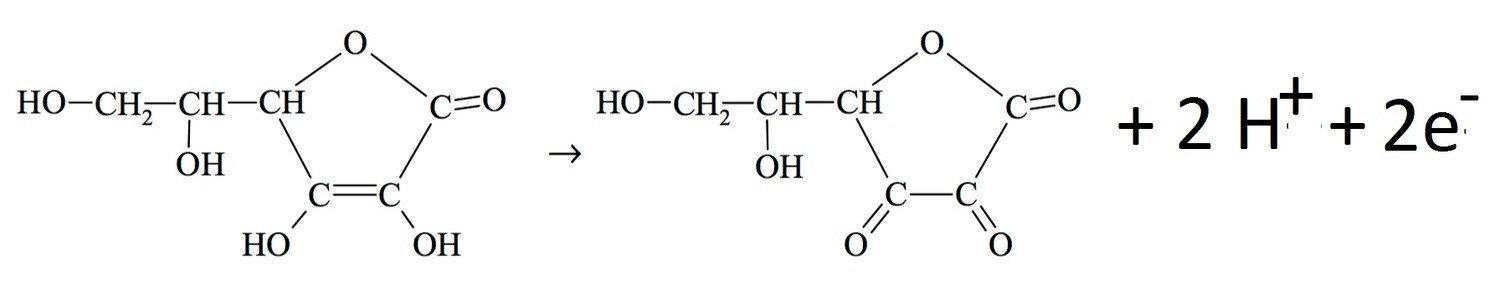
2e- + 1/2 O2 + 2H+ -> H2O
Zadanie 38-39.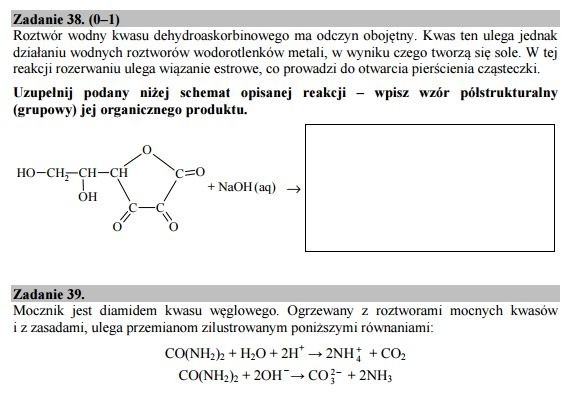

Odpowiedź:
Zadanie 38.
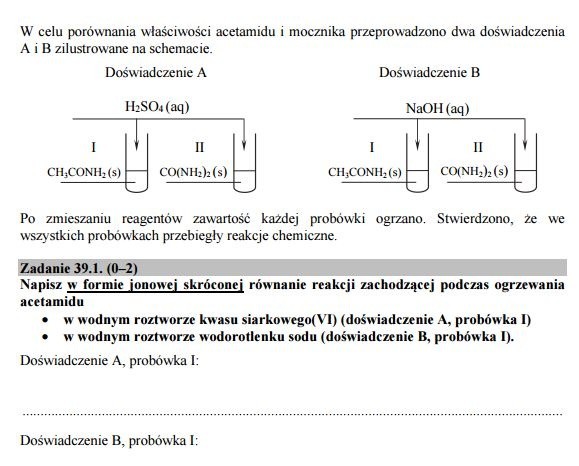
Zadanie 39. 1
Doświadczenie A, probówka I: CH3CONH2 + H2O + H+ -> CH3COOH + NH4+ (1 pkt)
Doświadczenie B, probówka I: CH3CONH2 + OH- -> CH3COO- + NH3
Zadanie 39.2
doświadczenie A
Probówka I: w probówce I wyczuwalny jest zapach octu, w probówce II wydziela się bezbarwny gaz
Probówka II: w obu probówkach wydziela się NH3
Zadanie 40-41.
Odpowiedź:
Zadanie 40.
1 PRAWDA
2. FAŁSZ
3. PRAWDA
Zadanie 41.
Gly-His-Lys
Uwaga na Instagram - nowe oszustwo
Dołącz do nas na Facebooku!
Publikujemy najciekawsze artykuły, wydarzenia i konkursy. Jesteśmy tam gdzie nasi czytelnicy!
Dołącz do nas na X!
Codziennie informujemy o ciekawostkach i aktualnych wydarzeniach.
Kontakt z redakcją
Byłeś świadkiem ważnego zdarzenia? Widziałeś coś interesującego? Zrobiłeś ciekawe zdjęcie lub wideo?
![Matura 2016: CHEMIA rozszerzona [ODPOWIEDZI, ARKUSZ CKE]](https://d-art.ppstatic.pl/kadry/k/r/1/6f/66/57347f7d2b2e2_o_medium.jpg)










